Bảng hóa trị không thiếu, mới mẻ nhất?
Bảng hóa trị là 1 phần đặc biệt cần thiết vô công tác Hóa học tập. Tuy nhiên nhằm học tập nằm trong bảng hóa trị của những yếu tố hoặc bảng nguyên vẹn tử khối thì ko nên là vấn đề dễ dàng và đơn giản tuy nhiên yên cầu chúng ta học viên cần thiết cần mẫn và với cơ hội học tập phải chăng.
Bảng hóa trị một vài yếu tố chất hóa học thịnh hành như sau:
Số proton | Tên Nguyên tố | Ký hiệu hoá học | Nguyên tử khối | Hoá trị |
1 | Hiđro | H | 1 | I |
2 | Heli | He | 4 | |
3 | Liti | Li | 7 | I |
4 | Beri | Be | 9 | II |
5 | Bo | B | 11 | III |
6 | Cacbon | C | 12 | IV, II |
7 | Nitơ | N | 14 | II, III, IV… |
8 | Oxi | O | 16 | II |
9 | Flo | F | 19 | I |
10 | Neon | Ne | 20 | |
11 | Natri | Na | 23 | I |
12 | Magie | Mg | 24 | II |
13 | Nhôm | Al | 27 | III |
14 | Silic | Si | 28 | IV |
15 | Photpho | P | 31 | III, V |
16 | Lưu huỳnh | S | 32 | II, IV, VI |
17 | Clo | Cl | 35,5 | I,… |
18 | Argon | Ar | 39,9 | |
19 | Kali | K | 39 | I |
20 | Canxi | Ca | 40 | II |
24 | Crom | Cr | 52 | II, III |
25 | Mangan | Mn | 55 | II, IV, VII… |
26 | Sắt | Fe | 56 | II, III |
29 | Đồng | Cu | 64 | I, II |
30 | Kẽm | Zn | 65 | II |
35 | Brom | Br | 80 | I… |
47 | Bạc | Ag | 108 | I |
56 | Bari | Ba | 137 | II |
80 | Thuỷ ngân | Hg | 201 | I, II |
82 | Chì | Pb | 207 | II, IV |
Chú thích:
- Nguyên tố phi kim: chữ color xanh
- Nguyên tố kim loại: chữ color đen
- Nguyên tố khí hiếm: chữ color đỏ
Ngoài rời khỏi, chúng ta học viên còn hoàn toàn có thể xác lập hóa trị theo gót bảng tuần trả những yếu tố chất hóa học như sau:
Bảng tuần trả chất hóa học mang đến học viên lớp 8:
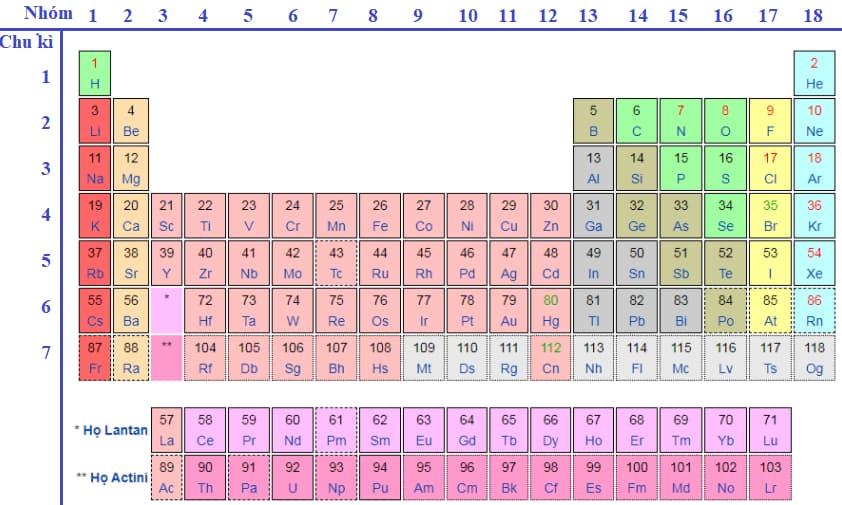
Bảng tuần trả chất hóa học mang đến học viên lớp 9:
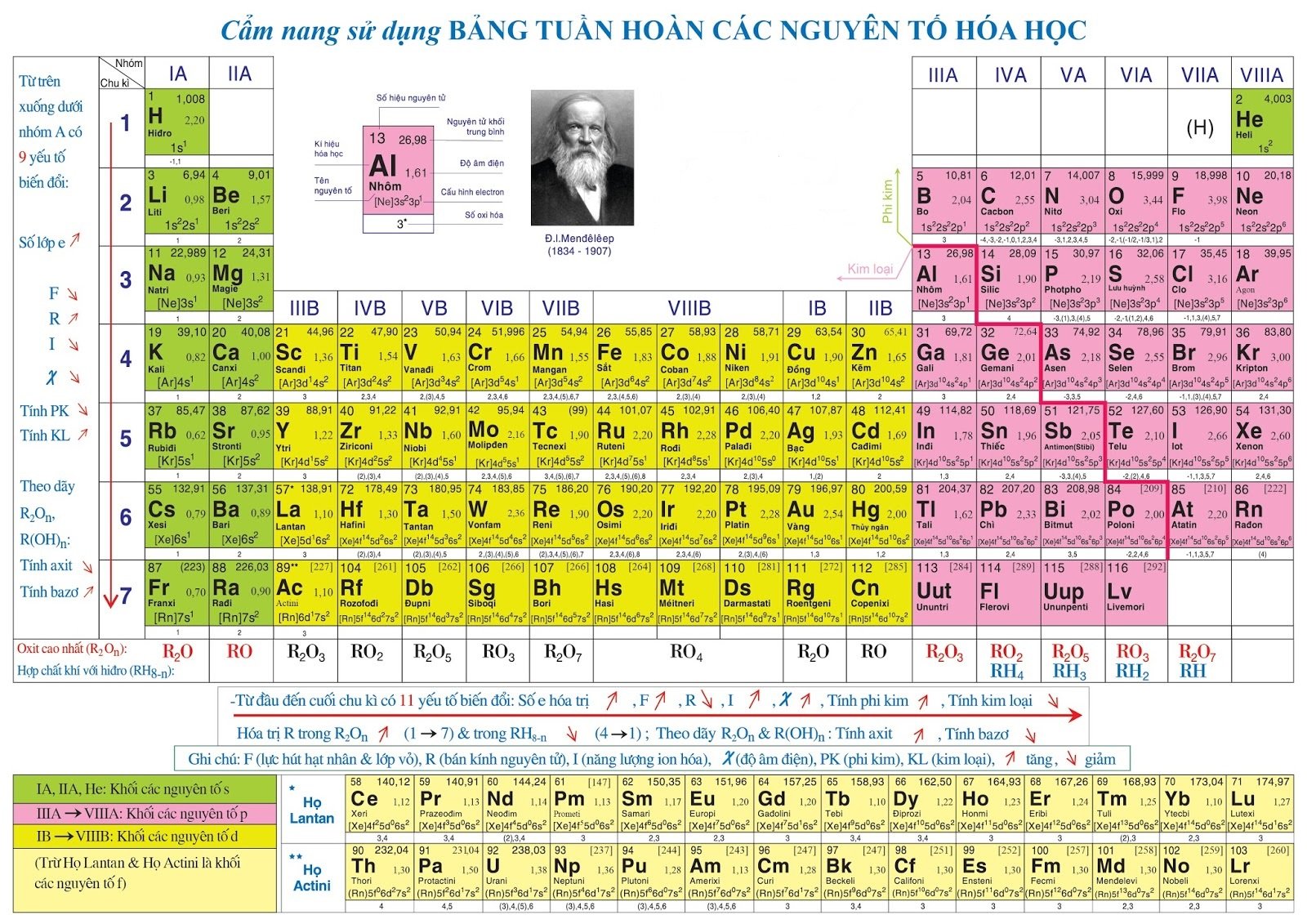
Bảng tuần trả yếu tố chất hóa học lớp 10 như sau:
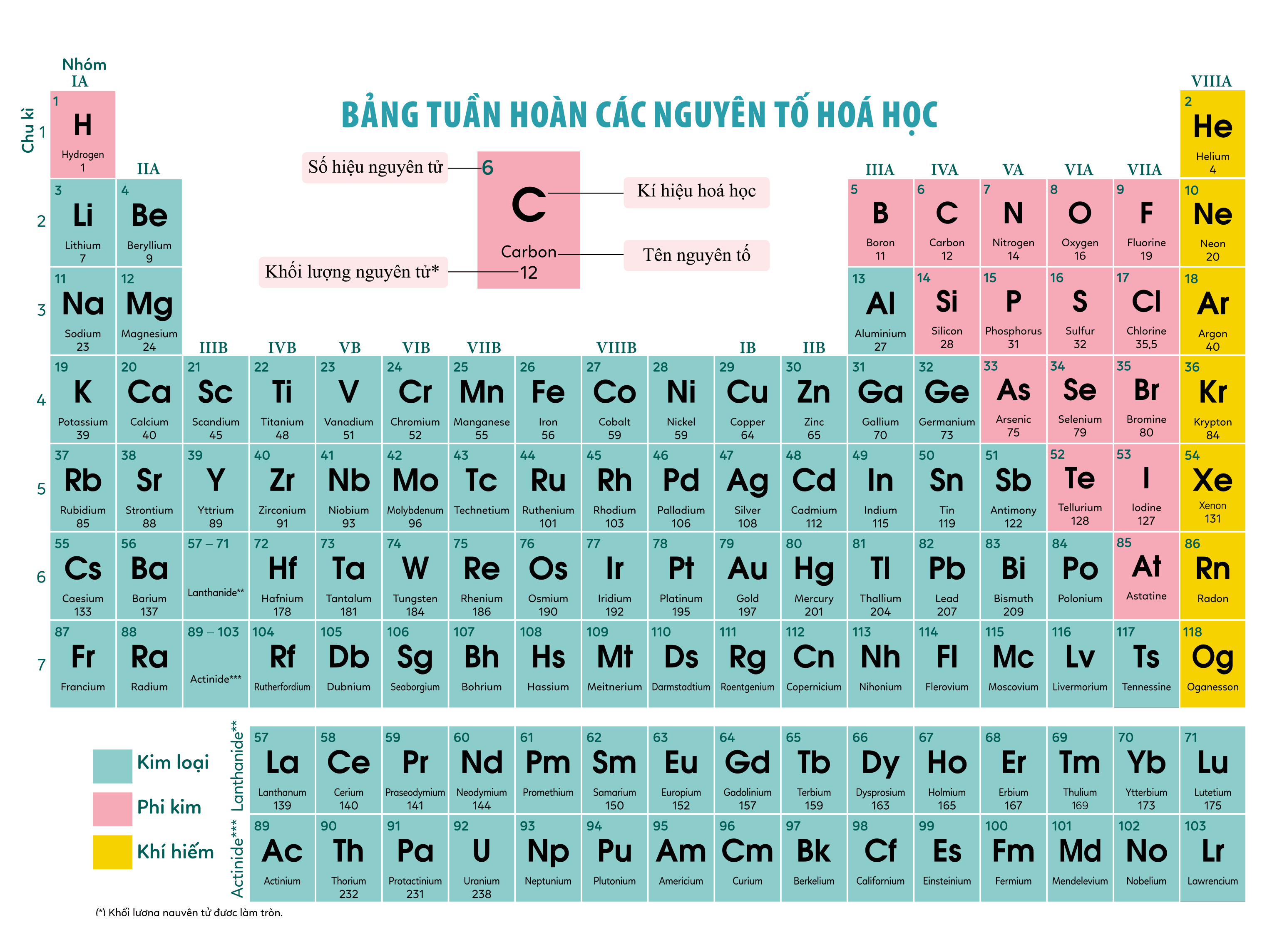
Lưu ý: Cách Bảng hóa trị, Bảng tuần trả những yếu tố chất hóa học bên trên chỉ mang tính chất hóa học tham lam khảo!
Xem thêm: Đảo ngữ là gì? Ví dụ câu hòn đảo ngữ
Xem thêm: 7 hằng đẳng thức xứng đáng nhớ? Cách hiểu 7 hằng đẳng thức kỷ niệm bởi vì điều cụt gọn
Xem thêm: Điệp ngữ là gì mang đến ví dụ? Tác dụng của điệp ngữ? Các loại phương án tu kể từ điệp ngữ
Bảng hóa trị đẩy đầy đủ, mới mẻ nhất? Bài ca hóa trị cụ thể, dễ dàng lưu giữ theo gót công tác mới mẻ như vậy nào? (Hình kể từ Internet)
Bài ca hóa trị cụ thể, dễ dàng lưu giữ theo gót công tác mới?
Các bài bác ca hóa trị và nguyên vẹn tử khối cụ thể, dễ dàng lưu giữ như sau:
Bài ca hóa trị số 1
Kali, Iôt, Hiđro
Natri với bạc, Clo một loài
Có hóa trị 1 các bạn ơi
Nhớ ghi mang đến rõ ràng kẻo rồi phân vân
Magiê, chì, Kẽm, thủy ngân
Canxi, Đồng ấy cũng xấp xỉ Bari
Cuối nằm trong thêm thắt chú Oxi
Hóa trị 2 ấy với gì khó khăn khăn
Bác Nhôm hóa trị 3 lần
Ghi sâu sắc trí lưu giữ khi cần phải có ngay
Cacbon, Silic này đây
Là hóa trị 4 ko thời buổi này quên
Sắt bại kể cũng quen thuộc tên
2, 3 tăng giảm thiệt phiền lắm thay
Nitơ phiền nhiễu nhất đời
1, 2, 3, 4 khi thời loại 5
Lưu huỳnh lắm khi nghịch tặc khăm
Xuống 2, lên 6 khi ở loại 4
Photpho rằng cho tới ko dư
Nếu ai căn vặn cho tới thì hừ rằng 5
Em ơi nỗ lực học tập chăm
Bài ca hóa trị xuyên suốt năm đặc biệt cần
Bài ca hóa trị số 2
Hidro (H) cùng theo với liti (Li)
Natri (Na) cùng theo với kali (K) chẳng tách Dường như còn bạc (Ag) sáng sủa ngời
Chỉ đem hoá trị I thôi chớ nhầm
Riêng đồng (Cu) cùng theo với thuỷ ngân (Hg)
Thường II không nhiều I chớ lăn tăn gì
Đổi thay cho II , IV là chì (Pb)
Điển hình hoá trị của chì là II
Bao giờ nằm trong hoá trị II
Là ôxi (O) , kẽm(Zn) chẳng sai chút gì
Ngoài rời khỏi còn tồn tại can xi (Ca)
Magiê (Mg) cùng theo với bari (Ba) một nhà
Bo (B) , nhôm (Al) thì hóa trị III
Cácbon C Silic (Si) thiếc (Sn) là IV thôi
Thế tuy nhiên nên rằng thêm thắt lời
Hóa trị II vẫn chính là điểm lên đường về
Sắt (Fe) II toan tính bộn bề
Không bền nên dễ dàng biến đổi ngay lập tức Fe III
Phốtpho III không nhiều gặp gỡ mà
Photpho V chủ yếu người tớ gặp gỡ nhiều
Nitơ (N) hoá trị từng nào ?
I , II, III , IV phần nhiều cho tới V
Lưu huynh lắm khi nghịch tặc khăm
Khi II khi IV , VI tăng tột cùng
Clo Iot lung tung
II III V VII thông thường thì I thôi
Mangan phiền nhiễu nhất đời
Đổi kể từ I cho tới VII thời mới mẻ yên
Hoá trị II người sử dụng đặc biệt nhiều
Hoá trị VII cũng khá được yêu thương hoặc cần
Bài ca hoá trị nằm trong lòng
Viết thông công thức dự phòng lãng quên
Học hành nỗ lực cần thiết chuyên
Siêng ôn thường xuyên luyện tất yếu lưu giữ nhiều
Bài ca hóa trị theo gót công tác mới
Chlo-rine (Cl), Po-tas-si-um (K)
Hy-dro-gen (H), So-di-um (Na), Sil 0 vẻ (Ag)
Và I-o (d) -dine nữa cơ
Đều nằm trong hóa trị một (I) nha từng người
Mag-ne(s)-si-um (Mg), cop-per (Cu)
Ba-ri-um (Ba), Zinc (Zn), Lead (Pb), Mer-cu-ry (Hg)
Cal-ci-um (Ca), O-xy-gen (O)
Hóa trị nhì (II) ấy với phần dễ dàng hơn
Bác a-lu-mi-ni-um (Al)
Hóa trị là (III) ghi tâm xung khắc cốt
Car-bon (C) và Si-li-con (Si)
Là hóa trị tứ (IV) khi cần thiết chớ quên
Ni-tro-gen (N) phiền nhiễu hơn
Một nhì phụ vương tứ (I, II, III, IV) khi thì năm (V)
Sul -fur (S) lắm khi nghịch tặc khăm
Lúc nhì (II), khi sáu (VI) khi ở loại tư (IV)
Phos-pho-rus (P) nhắc ko dư
Nội dung ví dụ và đòi hỏi cần thiết đạt của học viên lớp 10 lúc học Cấu tạo nên của bảng yếu tố tuần trả là gì?
Theo Chương trình dạy dỗ phổ thông môn Hóa học tập được phát hành tất nhiên Thông tư 32/2018/TT-BGDĐT quy lăm le nội dung ví dụ và đòi hỏi cần thiết đạt của học viên lớp 10 lúc học như sau:
- Nêu được về lịch sử vẻ vang sáng tạo lăm le luật tuần trả và bảng tuần trả những yếu tố hoá học tập.
- Mô mô tả được kết cấu của bảng tuần trả những yếu tố hoá học tập và nêu được những định nghĩa tương quan (ô, chu kì, nhóm).
- Nêu được phương pháp bố trí của bảng tuần trả những yếu tố hoá học tập (dựa theo gót thông số kỹ thuật electron).
- Phân loại được yếu tố (dựa theo gót thông số kỹ thuật electron: yếu tố s, p, d, f; dựa trên đặc thù hoá học: sắt kẽm kim loại, phi kim, khí hiếm).
